Fenoles y Alcoholes
Marco Teórico
Fenoles
Los fenoles como dijimos, son compuestos que resultan de reemplazar un hidrógeno o más de su anillo aromático por uno o más OH.El miembro más simple e importante de esta familia es el hidroxibenceno o Fenol.
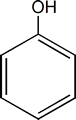
Si existen 2, 3 o más grupos OH se denominaran difenoles, trifenoles o polifenoles respectivamente. Cuando los sustituyentes del anillo estan vecinos se los llama con el prefijo orto (o). Si hay un lugar de separación entre ellos es meta (m) y si estan en lados opuestos para (p).
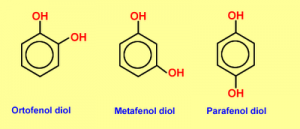
El fenol no existe en estado libre.Se forma en la destilación seca de la hulla. Luego se destilan los aceites medios del alquitrán de hulla.Por este método se obtiene poca cantidad. Por este motivo se lo prepara hoy sintéticamente. A partir de la formación del ácido bencenosulfónico:
En la primera etapa el benceno reacciona con el ácido sulfúrico:
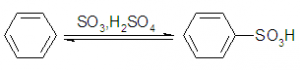
Este ácido formado después reacciona con el sulfito de sodio, dando como producto bencenosulfonato de sodio.
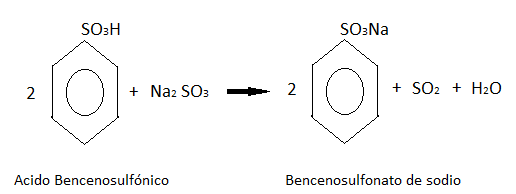
El bencenosulfonato de sodio después se concentra por evaporación y se combina con hidróxido de sodio
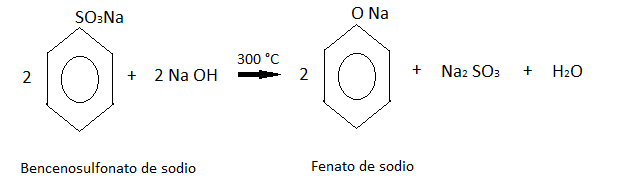
Este último producto se acidifica con dióxido de azufre de una de las reacciones anteriores, obteniendo finalmente al fenol.
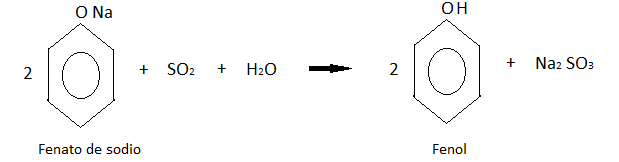
Propiedades del fenol
Es un sólido que cristaliza como agujas incoloras de olor particular. Su temperatura de fusión es de 38°C y su punto de ebullición de 181°C. es higroscópico, es decir, absorbe mucha agua.Se puede oxidar ante la luz adquiriendo una coloración rosada. Es cáustico.Es poco soluble en agua. Muy soluble en éter y alcohol.Químicamente se comporta como ácido débil. Produce por lo tanto iones hidrógeno al disociarse.Con respecto a las reacciones, hay de dos tipos. Las que se relacionan con el grupo OH y aquellas en las que participa el anillo.
Formación de sales: El fenol al ser un ácido débil, reacciona con facilidad con una base fuerte como la del sodio, litio o potasio.
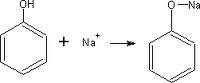
Esta reacción si bien las presentan los alcoholes alifáticos, es más débil en estos. En el caso del fenol se da con mayor tendencia.
Formación de éteres: Los fenatos de sodio se tratan con halogenuros de alquilo. En este caso particular con cloruro de metilo, obteniendo el éter feniletílico como indica la reacción.
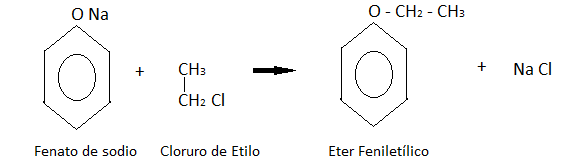
Entre las reacciones del anillo aromático, es decir, de sustitución, podemos nombrar las principales.
Halogenación:
Haciendo reaccionar al fenol con cloro, por ejemplo, se obtiene una mezcla de o-clorofenol y p-clorofenol.
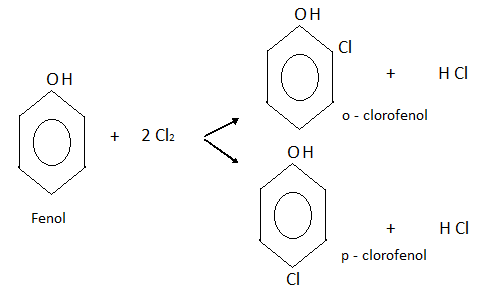
Sulfonación:
El fenol se puede combinar con el ácido sulfúrico en caliente, dando una mezcla de dos isómeros de ácido o-fenol sulfónico y p-fenol sulfónico.
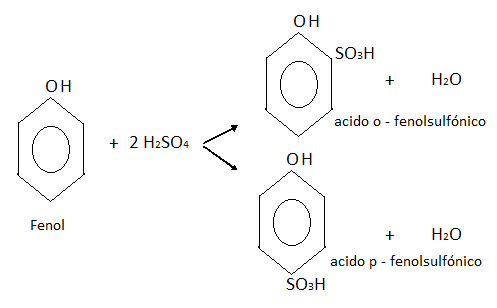
Nitración:
En este caso también se obtiene una mezcla de dos isómeros, o-nitrofenol y p-nitrofenol.
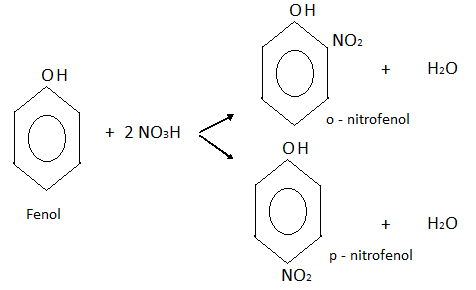
Alcoholes
Los alcoholes son un grupo de moleculas organicas caracterizadas por la presencia de uno o mas grupos -OH (hidroxilo) como grupo principal. Los alcoholes tienen de formula general: R-OH, estructuralmente son semejantes al agua, en donde uno de los hidrógenos se ha sustituido por un grupo alquilo. Su grupo funcional es el grupo hidroxilo, OH.
se divide en Alcoholes primarios, secundarios y terciarios.
Un alcohol es primario, si el átomo de hidrogeno (H) sustituido por el grupo oxidrilo (-OH) pertenece a un carbón (C) primario:
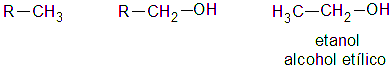
Es secundario, si el átomo de hidrogeno (H) sustituido por el grupo oxidrilo (-OH) pertenece a un carbón (C) secundario:
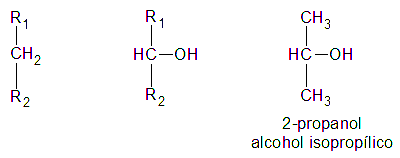
Finalmente, es terciario, si el átomo de hidrogeno (H) sustituido por el grupo oxidrilo (-OH) pertenece a un carbón (C) terciario:
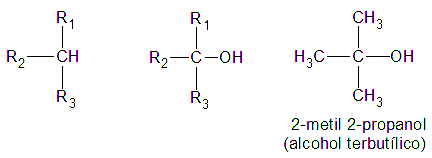
La función alcohol puede repetirse en la misma molécula, resultando monoles, o alcoholes monovalentes; dioles, o alcoholes bivalentes; trioles, o alcoholes trivalentes, etc.
Fórmula
|
Nombre
|
Clasificación
|
 |
1-propanol
|
monol
|
 |
1,2-propanodiol(propilen glicol)
|
diol
|
 |
1,2,3-propanotriol(glicerina)
|
triol
|
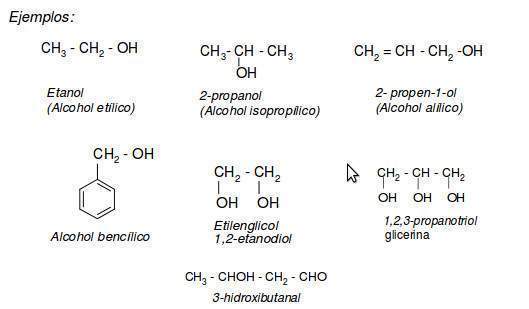
Nomenclatura alcoholes
En la nomenclatura de alcoholes se suelen emplear nombres vulgares para los términos más sencillos ( C1 - C4 ). Estos nombres se forman con la palabra alcohol.
El sistema IUPAC nombra a los alcoholes de acuerdo a las siguientes reglas:
- Se busca la cadena más larga que incluya el Grupo Hidroxilo. La terminación o del hidrocarburo se cambia por -ol.
- La cadena se numera de forma que al grupo funcional le corresponda el menor número posible. Si hay mas de un grupo hidroxilo en la cadena, se emplean los prefijos di, tri, etc.
- Cuando el alcohol no es el grupo funcional principal se nombra como hidroxi, precedido de su número localizador.
Propiedades alcohol
En cuanto a sus propiedades, los alcoholes de baja masa molecular, están a temperatura ambiente en estado líquido y son incoloros, además de solubles en agua en mayor o menor medida.
A medida que aumenta el tamaño de la molécula también aumenta su punto de fusión y baja su solubilidad en el agua, llegando a poder estar en algunos casos en estado solido a temperatura ambiente. Aunque la mayoría de alcoholes tienen una densidad menor que la del agua, algunos, especialmente los que cuentan con anillos aromáticos, poseen una densidad mayor. La polaridad de los grupos -OH permite a estas moléculas establecer enlaces puente de hidrógeno con moléculas compañeras, o con aniones.
EJERCICIOS DE ALCOHOLES Y FENOLES:
Webgrafia
https://es.wikipedia.org/wiki/Fenol
https://quimicayalgomas.com/quimica-organica/alcoholes-aldehidos-cetonas/alcoholes-parte-4/
https://www.alonsoformula.com/organica/fenois.htm
https://es.wikipedia.org/wiki/Alcohol
https://www.alonsoformula.com/organica/alcohois.htm
http://www.100ciaquimica.net/f
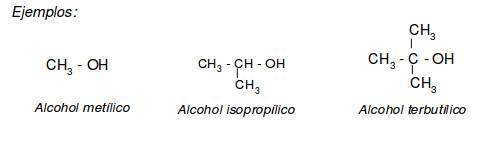


FALTÓ INTRODUCCIÓN Y OBJETIVOS 4,4
ResponderEliminar